La forma del agua - BIOVIA COSMO
- Detalles
- Categoría: BIOVIA
- Visto: 376
Entendiendo el efecto hidrofóbico
Aunque parezca bastante abstracto, las interacciones de moléculas y átomos a nivel microscópico a menudo tienen efectos profundos en las propiedades macroscópicas de los materiales y la vida misma.
El software de química de solvatación de BIOVIA proporciona el enlace científico para comprender estas conexiones entre las interacciones microscópicas y moleculares y las propiedades experimentales relevantes para la industria de los líquidos, como las solubilidades, las presiones de vapor, los coeficientes de partición y muchas más. De manera ejemplar, en esta entrada del blog, queremos discutir el efecto hidrofóbico anómalo del agua a nivel molecular y sus implicaciones en las aplicaciones industriales y la vida en la Tierra en general.
El fenómeno conocido como efecto hidrofóbico, originario de las palabras griegas ύδωρ (ydor, agua) y φόβος (phobos, miedo), describe cómo las moléculas que "temen" al agua, tienden a unirse para evitar interactuar con ella. Este efecto explica por qué el aceite y el agua no se mezclan, sino que forman fases separadas, o por qué algunos compuestos son mejor solubles en agua que otros.
No se trata solo de un conocimiento árido de los libros de texto, sino de un concepto fundamental para la existencia de la vida en nuestro planeta, que sirve como un impulsor clave detrás de procesos biológicos como la formación de células y el plegamiento de proteínas en estructuras activas o inactivas. Las proteínas son bloques de construcción esenciales de nuestro cuerpo, que consisten en cadenas de aminoácidos. En muchos casos, las proteínas solo funcionan correctamente cuando están en un cierto estado plegado, un estado que generalmente se logra dentro de un rango específico de temperaturas. Entre otros factores, el aumento de las temperaturas puede provocar la desnaturalización de las proteínas, dejándolas inactivas. Este proceso se puede observar fácilmente, por ejemplo, al hervir un huevo, donde la albúmina de huevo se convierte en una sustancia blanca y opaca tras la desnaturalización de las proteínas (principalmente la ovoalbúmina) por encima de 60 ° C. También a temperaturas más bajas, las proteínas pueden sufrir un despliegue reversible, un proceso conocido como desnaturalización en frío. Este comportamiento está directamente relacionado con la sensibilidad a la temperatura del efecto hidrofóbico y, para entenderlo, es necesario investigar la hidrofobicidad del agua en sí.
La sorprendente hidrofobicidad del agua
Puede sonar sorprendente, pero el agua en sí misma puede ser hidrofóbica, al menos hasta cierto punto.
Las moléculas de agua pueden estar dispuestas en formas o grupos específicos. Aquí, las moléculas están conectadas por lo que los químicos llaman un enlace de hidrógeno. En el agua, este tipo especial de enlace se produce entre un átomo de hidrógeno y el átomo de oxígeno de otra molécula de agua. Dado que el agua tiene dos átomos de hidrógeno y cada átomo de oxígeno puede acomodar dos enlaces de hidrógeno, se pueden formar redes complejas que estabilizan diferentes formas de grupos de agua. Curiosamente, la superficie de estos grupos tiene propiedades diferentes a la superficie de las moléculas de agua individuales.
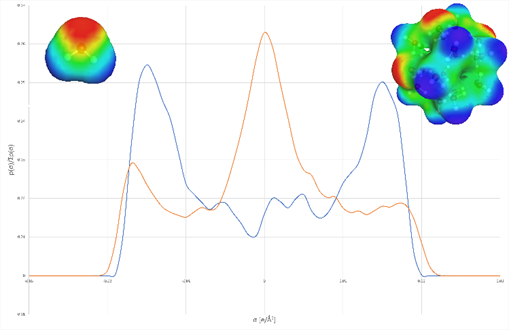
Perfil de densidad de carga de cribado relativo de la superficie de una sola molécula de agua (azul, estructura arriba a la izquierda) y un grupo de 20 moléculas (naranja, estructura arriba a la derecha). Claramente es visible el pico del área neutra de carga en el centro de la curva naranja, que está ausente para las moléculas de agua aisladas.
La imagen muestra la superficie de densidad de carga del agua y un grupo de moléculas de agua conectadas por enlaces de hidrógeno, fácilmente calculables con BIOVIA Turbomole. Las áreas azules y rojas denotan áreas de superficie con grandes densidades de carga de cribado positivas o negativas, mientras que las áreas verdes denotan pequeñas densidades de carga de cribado cercanas a cero. Generalmente, como consecuencia directa de la ley de Coulomb, las cargas opuestas se atraen entre sí. Por lo tanto, los compuestos con grandes densidades de carga de cribado positivas o negativas, prefieren estar en contacto con compuestos de densidades de carga de cribado opuestas coincidentes. Los compuestos con una gran cantidad de área de superficie no polar (verde) prefieren otros compuestos no polares. Como se puede ver, el agua en sí misma tiene bastantes densidades de carga de cribado positivas y negativas (azul, rojo). En contraste con esto, la estructura del grupo tiene un área más neutra con pequeñas densidades de carga de cribado. Por esta razón, estos grupos se comportan en parte como una sustancia hidrofóbica no polar.
Por lo tanto, a bajas temperaturas, cuando estos grupos se vuelven más estables, las propiedades superficiales del agua cambian. El agua misma se vuelve cada vez más hidrofóbica y, a su vez, las moléculas hidrofóbicas se vuelven más solubles en agua. Cuando la temperatura aumenta, los grupos se rompen y la solubilidad de las moléculas hidrofóbicas disminuye. A temperaturas aún más altas, otros efectos termodinámicos vuelven a aumentar la solubilidad, lo que lleva a un mínimo de solubilidad, que normalmente se encuentra en algún lugar en el rango de 20 a 80 °C, es decir, cerca de la temperatura ambiente y corporal.
La evaluación precisa de esta dependencia de la temperatura es importante en muchas aplicaciones, que van desde la solubilidad de los aditivos en el procesamiento de petróleo o las aplicaciones de captura de carbono, hasta el cálculo de los coeficientes de partición de los ingredientes farmacéuticos activos.
Avanzando en la innovación con BIOVIA COSMOtherm
BIOVIA COSMOtherm permite simular el efecto hidrofóbico dependiente de la temperatura del agua de una manera eficiente y precisa, como se muestra en una reciente publicación de M. P. Andersson y M. Richter
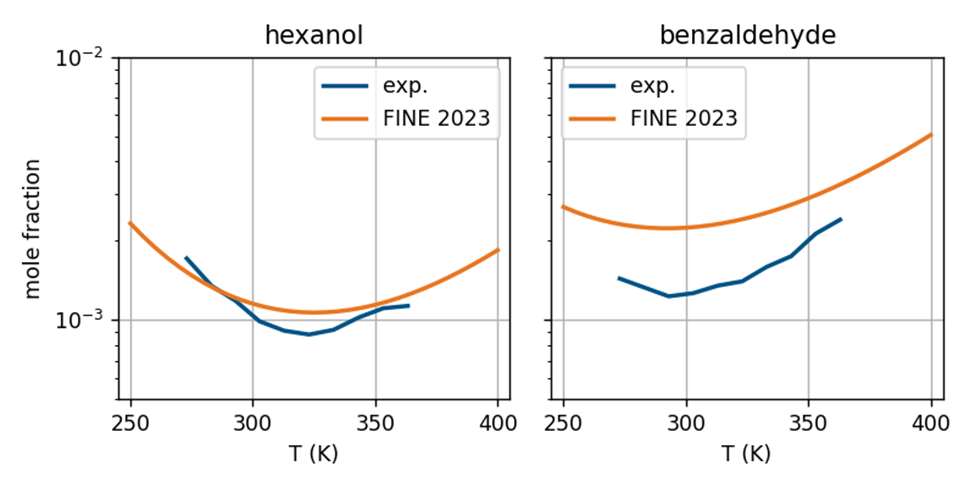
Se muestran las solubilidades acuosas de hexanol y benzaldehído en un amplio rango de temperaturas. Las solubilidades experimentales (curvas azules) muestran un mínimo alrededor de 320 K (hexanol) y 290 K (benzaldehído) debido al efecto hidrofóbico del agua. COSMOtherm FINE 2023 es capaz de recuperar estos mínimos con alta precisión (325 K para el hexanol y 290 K para el benzaldehído).
La imagen muestra la solubilidad dependiente de la temperatura del hexanol y el benzaldehído en agua. Dado que ambos compuestos son bastante hidrofóbicos, la solubilidad es generalmente bastante pequeña, pero la simulación y el experimento muestran claramente un mínimo de solubilidad alrededor de 290 K (17 °C) para el benzaldehído y 320 K (47 °C) para el hexanol. Con BIOVIA COSMOtherm la solubilidad dependiente de la temperatura de cualquier compuesto en agua se puede evaluar fácilmente de inmediato, incluidas anomalías como el efecto hidrofóbico del agua. Esta capacidad permite realizar cribados in silico a gran escala de las propiedades moleculares con alta precisión que complementan los esfuerzos experimentales, aceleran la innovación y reducen el tiempo de comercialización para nuestros clientes.

